Νόσος von HIPPEL-LINDAU
Η Νόσος Von
Hippel-Lindau (VHL) είναι ένα σπάνιο, κληρονομικό, πολυσυστηματικό σύνδρομο που
προδιαθέτει σε ανάπτυξη καλοηθών και κακοηθών όγκων σε διάφορα όργανα Η νόσος VHL επηρεάζει πολλά όργανα,
συμπεριλαμβανομένης της παρεγκεφαλίδας, του νωτιαίου μυελού, του
αμφιβληστροειδούς, του νεφρού, του παγκρέατος και της επιδιδυμίδας.
ΑΙΤΙΑ
Προκύπτει από
μια αυτοσωμική επικρατή μετάλλαξη που επηρεάζει ένα γονίδιο καταστολής όγκων,
VHL, που εντοπίζεται στο χρωμόσωμα
3p25.3 . Περίπου το 80% των ατόμων με σύνδρομο von Hippel-Lindau έχουν έναν
πάσχοντα γονέα και περίπου το 20% έχει μια de novo γονιδιακή μετάλλαξη.
Διατίθενται μοριακές εξετάσεις που ανιχνεύουν μεταλλάξεις σε σχεδόν το 100% των
ασθενών.
Το γονίδιο
VHL είναι ογκοκατασταλτικό → ρυθμίζει την αποδόμηση του HIF-1α → απορρύθμιση
αγγειογένεσης, κυτταρικής αύξησης και υποξικής απάντησης
ΕΠΙΔΗΜΙΟΛΟΓΙΑ
Η συχνότητά
της είναι περίπου 1 στα 36.000 νεογνά.
ΤΑΞΙΝΟΜΗΣΗ
Η νόσος VHL
υποκατηγοριοποιείται στον:
-τύπο 1, που
χαρακτηρίζεται από HAB και RCC χωρίς PHEO
-τύπο 2Α, που
χαρακτηρίζεται από PHEO και HAB χωρίς RCC
-τύπο 2B, που
χαρακτηρίζεται από PHEO και HAB με RCC
-τύπο 2C, που
χαρακτηρίζεται από αποκλειστική ανάπτυξη του PHEO
-τύπο 3, που
χαρακτηρίζεται από την ανάπτυξη πολυκυτταραιμίας χωρίς αυξημένη καρκινική
προδιάθεση.
Συγκεκριμένα,
παρά τη φαινοτυπική ετερογένεια, η νόσος VHL προκαλείται από μετάλλαξη ή
απώλεια ενός μόνο γονιδίου, του VHL.
ΠΑΘΟΦΥΣΙΟΛΟΓΙΑ
Το φυσιολογικό VHL γονίδιο (VHL protein / pVHL)
-
Το γονίδιο VHL κωδικοποιεί για την πρωτεΐνη pVHL.
-
Η pVHL σχηματίζει σύμπλοκο (VBC complex: VHL, elongin B & C, cullin-2, RBX1).
-
Ο ρόλος του συμπλόκου: ουβικιτινυλίωση και αποδόμηση του HIF-α (Hypoxia-Inducible Factor α) σε φυσιολογικές οξυγονικές συνθήκες.
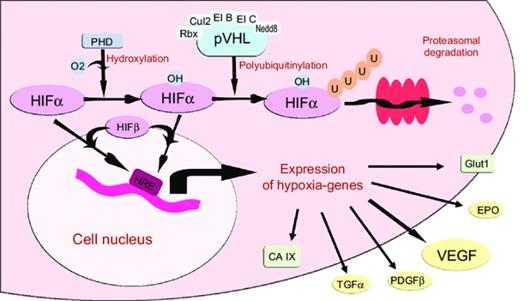
Η pVHL είναι το υπόστρωμα αναγνώρισης μιας πολυπρωτεϊνικής E3 λιγάσης ουβικιτίνης ECV (Elongins BC/Cul2/VHL) που στοχεύει την α-υπομονάδα του επαγώγιμου από την υποξία παράγοντα (HIF) για ουβικιτυλίωση υπό κανονική τάση οξυγόνου. O HIF-α υδροξυλιώνεται σε διατηρημένες προλίνες εντός του οξυγονο-εξαρτώμενου τομέα αποικοδόμησης (ODD) από μια οικογένεια ενζύμων προλυλικής υδροξυλάσης (PHD1-3) παρουσία 2-οξογλουταρικού, σιδήρου και οξυγόνου. H pVHL συνδέεται αποκλειστικά με προλυλ υδροξυλιωμένο HIF.
Υπό φυσιολογικές συνθήκες (νορμοξία):
-
Ο HIF-α (κυρίως HIF-1α & HIF-2α) υδροξυλιώνεται (prolyl hydroxylase enzymes).
-
Η υδροξυλιωμένη μορφή του HIF-α αναγνωρίζεται από το pVHL.
-
Το pVHL ουβικιτινυλιώνει τον HIF-α → αποδόμηση από το πρωτεοσωμάτιο.
-
Έτσι, κρατιέται σε χαμηλά επίπεδα → φυσιολογική ρύθμιση αγγειογένεσης.
Σε υποξία
Σε υποξία ή βλάβη του VHL γονιδίου:
-
Δεν γίνεται υδροξυλίωση → ο HIF-α ΔΕΝ αναγνωρίζεται από το pVHL.
-
Ο HIF-α σταθεροποιείται → μετακινείται στον πυρήνα → ενεργοποιεί γονίδια στόχους.
Απορρύθμιση HIF → Υπερδραστηριότητα διαφόρων οδών:
| Οδός | Παράγοντας | Αποτέλεσμα |
|---|---|---|
| Αγγειογένεση | VEGF | Αγγειακή υπερπλασία, αιμαγγειοβλαστώματα |
| Κυτταρική αύξηση | PDGF, TGF-α | Προώθηση όγκων |
| Γλυκόλυση | GLUT1 | Αυξημένη πρόσληψη γλυκόζης |
| Κυτταρική επιβίωση | EPO | Αυξημένη παραγωγή ερυθρών |
Έτσι, σε υποξία, το μη τροποποιημένο HIF1-a διαφεύγει της αναγνώρισης από το VHL και ετεροδιμερίζεται με το συστατικά εκφραζόμενο HIF1-b (& HIF-2a) για να σχηματίσει έναν ενεργό μεταγραφικό παράγοντα, ο οποίος ενεργοποιεί πολυάριθμα επαγόμενα από υποξία γονίδια που εμπλέκονται σε διάφορες προσαρμοστικές διεργασίες όπως είναι ο αναερόβιος μεταβολισμός, η αγγειογένεση και η ερυθροποίηση. Λαμβάνοντας υπόψη την ευρεία φαινοτυπική μεταβλητότητα στη νόσο VHL, μια πρόβλεψη ήταν ότι το ECV είχε περισσότερα από ένα υπόστρωματα. Τα τελευταία χρόνια, αρκετές πρωτεΐνες έχουν αναφερθεί ότι είναι υποστρώματα πρωτεϊνών που σχετίζονται με ECV ή VHL, όπως RBP1, aPKC, SPRY2 και 2AR. Ωστόσο, η βιολογική ή παθοφυσιολογική σημασία τέτοιων αλληλεπιδράσεων στο πλαίσιο της νόσου VHL παρέμεινε σε μεγάλο βαθμό ασαφής. Αντίθετα, μελέτες έχουν προτείνει ότι η απορρύθμιση του HIF μετά τη μετάλλαξη ή την απώλεια του VHL συμβάλλει στην ανάπτυξη της νόσου VHL, ιδιαίτερα του HAB και του RCC, αλλά δεν φαίνεται να εμπλέκεται στην ανάπτυξη του PHEO. Περιέργως, η δέσμευση με την πρωτεΐνη εξωκυτταρικής ουσίας φιμπρονεκτίνη χάθηκε σε όλα τα μεταλλάγματα VHL που προκαλούν νόσους που δοκιμάστηκαν μέχρι σήμερα. Ωστόσο, η βιολογική σημασία αυτής της χαμένης αλληλεπίδρασης ή η συμβολή της, εάν υπάρχει, στη συσχέτιση γονότυπου-φαινοτύπου στη νόσο VHL παραμένει αναπάντητη.
Συνολικός παθοφυσιολογικός αντίκτυπος:
-
Πολυεστιακή νεοπλασία (νεφροκυτταρικός καρκίνος, φαιοχρωμοκύττωμα, PNETs)
Αγγειακή υπερπλασία (αιμαγγειοβλαστώματα)
-
Κυστικοί σχηματισμοί (νεφροί, πάγκρεας)
ΚΛΙΝΙΚΗ
ΕΙΚΟΝΑ
ΚΕΝΤΡΙΚΟ
ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ
Τα κύρια
νευρολογικά χαρακτηριστικά της πάθησης περιλαμβάνουν παρεγκεφαλιδικά
αιμαγγειοβλαστώματα και αγγειώματα αμφιβληστροειδούς (επίσης γνωστά
ως τριχοειδικά αιμαγγειοβλαστώματα αμφιβληστροειδούς-ΗΑΒ). Ασθενείς με
παρεγκεφαλιδικό αιμαγγειοβλάστωμα εμφανίζονται στην πρώιμη ενήλικη ζωή με
συμπτώματα και σημάδια αυξημένης ενδοκρανιακής πίεσης. Ένας μικρότερος αριθμός
ασθενών έχει αιμαγγειοβλάστωμα του νωτιαίου μυελού, προκαλώντας
ανωμαλίες στην ιδιοδεκτικότητα και διαταραχές στη βάδιση και τη λειτουργία της
ουροδόχου κύστης. Μια αξονική τομογραφία ή μαγνητική τομογραφία εγκεφάλου
συνήθως δείχνει μια κυστική παρεγκεφαλιδική βλάβη με αγγειακό
τοιχωματικό οζίδιο. Η ολική χειρουργική αφαίρεση του όγκου είναι θεραπευτική.
Περίπου το
25% των ασθενών με παρεγκεφαλιδικό αιμαγγειοβλάστωμα έχουν αγγειώματα
αμφιβληστροειδούς. Τα αγγειώματα αμφιβληστροειδούς χαρακτηρίζονται από
μικρές μάζες λεπτών τριχοειδών αγγείων που τροφοδοτούνται από μεγάλα και
ελικοειδή αρτηρίδια και φλεβίδια. Συνήθως βρίσκονται στον περιφερικό
αμφιβληστροειδή, έτσι ώστε η όραση να μην επηρεάζεται. Η έκκριση στην περιοχή
των αγγειωμάτων μπορεί να οδηγήσει σε αποκόλληση αμφιβληστροειδούς και απώλεια
όρασης. Τα αγγειώματα του αμφιβληστροειδούς αντιμετωπίζονται με φωτοπηξία και
κρυοπηξία, και και οι δύο έχουν δώσει καλά αποτελέσματα, αν και μπορεί να
εμφανιστούν επιπλοκές όπως οίδημα αμφιβληστροειδούς.
ΝΕΦΡΟΙ
Οι κυστικές
αλλοιώσεις των νεφρών, συσχετίζονται συχνά με τη νόσο von Hippel-Lindau,
ενώ το νεφρικό καρκίνωμα εκ διαυγών κυττάρων (RCC) είναι η πιο συχνή αιτία θανάτου
ΠΑΓΚΡΕΑΣ
Οι κύστες του
παγκρέατος και οι παγκρεατικοί νευροενδοκρινικοί όγκοι (PNETs) παρατηρούνται
στη νόσο von Hippel-Lindau
ΕΠΙΝΕΦΡΙΔΙΑ
Παρατηρείται φαιοχρωμοκύτωμα
(PHEO-αμφοτερόπλευρα
μερικές φορές)
ΑΛΛΑ
Κυσταδενώματα
της επιδιδυμίδας, κυστικές βλάβες του ήπατος, όγκος του ενδολεμφικού σάκου του
έσω ωτός
ΚΡΙΤΗΡΙΑ
ΔΙΑΓΝΩΣΗΣ
• ≥2 αιμαγγειοβλαστώματα ή
• 1 αιμαγγειοβλάστωμα + οικογενειακό
ιστορικό ή
• Γενετική επιβεβαίωση
ΔΙΑΓΝΩΣΗ
• Γενετικός έλεγχος VHL γονιδίου
• MRI εγκεφάλου, νωτιαίου μυελού, νεφρών, επινεφριδίων
• Οφθαλμολογική εξέταση (βυθοσκόπηση)
• Βιοχημικός έλεγχος για
φαιοχρωμοκύττωμα (μετανεφρίνες πλάσματος ή ούρων)
ΠΑΡΑΚΟΛΟΥΘΗΣΗ
Η τακτική
παρακολούθηση και οι κατάλληλες απεικονιστικές εξετάσεις είναι απαραίτητες για
τον εντοπισμό βλαβών που μπορούν να αντιμετωπιστούν σε πρώιμο στάδιο.
Σε
πάσχοντα άτομα ηλικίας 1 έτους και άνω,
θα πρέπει να γίνεται ετήσια αξιολόγηση της:
-
νευρολογικής κατάστασης
-της
όρασης/οφθαλμολογικής κατάστασης
-της ακοής
-της
αρτηριακής πίεσης.
Μετά την
ηλικία των 5 ετών, θα
πρέπει να γίνεται εργαστηριακός έλεγχος για
-φαιοχρωμοκύτωμα
κάθε χρόνο
-αξιολόγηση
της ακοής κάθε 2-3 χρόνια
-μαγνητική
τομογραφία με λεπτές τομές του εσω ακουστικού πόρου για την αξιολόγηση των
όγκων του ενδολεμφικού σάκου σε όσους έχουν συμπτώματα.
Μετά την
ηλικία των 16 ετών,
θα πρέπει να γίνεται :
-υπερηχογράφημα
κοιλίας ετησίως για τον εντοπισμό σπλαχνικών βλαβών
-μαγνητική
τομογραφία της κοιλίας και ολόκληρου του νευρικού άξονα κάθε 2 χρόνια.
ΑΝΤΙΜΕΤΩΠΙΣΗ
• Πολυεπιστημονική
παρακολούθηση
• Τακτικός
προληπτικός έλεγχος
• Χειρουργική
αφαίρεση όγκων όταν χρειάζεται
• Στοχευμένες
θεραπείες σε καρκίνο νεφρού (π.χ. VEGF αναστολείς)

Δεν υπάρχουν σχόλια:
Δημοσίευση σχολίου